电池原理
自1800年伏特发明了世界上第一个化学电源“伏打电堆”,电池技术便开始了200多年的发展历程。
当浸泡在溶液中被布隔开的铜和锌片用导线连接时,伏特先生感受到了电流的刺激,随着叠在一起的铜和锌片越多,电流的刺激感就变得越强。这就是伏特为我们带来的第一个电学能源装置。
然而,这里却有一个有趣的点:法拉第发现电磁感应定律是在1831年的事情,而1832年才出现第一台手摇式发电机,这意味着人类发电技术惠及民用还要经历很长的一段时间,即便1807年戴维发现了电解池(电池充电原理上就是电解池),显然人们也不会用原电池给原电池充电(科学研究除外)。所以我们发现,一开始出现的便是一次电池。这也决定了将有相当长的时间,科学家研究都是原电池——
比如1836年发明的第一个实用的电池——丹尼尔电池(锌铜原电池)。随后相当长的一段时间都没有出现实质意义上大规模商用的电池,直到——酸性锌锰干电池的商业化。
20世纪中期之前,原电池电解液容易泄漏的缺点阻碍了原电池的普及和商用。干电池技术利用某种吸收剂(如木屑或明胶)使电解液成为不会外溢的糊状,这样大大增强了电池的可携带性和便民性。
然而酸性锌锰干电池容易腐蚀锌金属产生氢气,导致电池膨胀,于是开发了碱性锌锰干电池,功率更好,容量更大,这便是我们至今还在经常使用的干电池。
以干电池为代表的一次电池经历了多次技术革新和商业化迭代,已经形成了价格优势,相对来说这些干电池原料成本较低,制造工艺成熟,习惯性的一次电池制造工艺便没有考虑重复使用的电池内部结构改造。
随着电池技术的进步,人们开始意识到:相对来说,二次电池循环使用时间更长,性价比更高,也更环保和节约资源,因此开始改造各种电池内部结构,使其成为二次电池,众多企业也在逐渐退出一次电池市场。
二次电池在材料角度最突出的特点就是反应可逆,这意味着完成一次放电和充电,要保证材料在成分和结构上的基本复原。
换句话说,充放电过程中电解质成分、电极结构是不改变的。接下来我们以最常见的碱性锌锰干电池和锂离子二次电池为例。
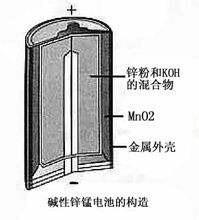
如图,碱性锌锰干电池以传统圆柱形结构,电解二氧化锰、石墨正极和氢氧化钾水溶液压入钢壳中,再插入纸隔膜网带或者两条条状物,锌粉的氢氧化钾胶体装入网带,集流体从底部插入。电解质还含有防止锌腐蚀的抑制剂。以上便是碱性锌锰干电池的材料,内部结构和制造工艺了。
该工艺中,负极是以均匀的锌粉存在的,当电池使用结束,以氧化锌形式析出。
如图,正极为橄榄石结构的磷酸铁锂材料,负极为层状结构的石墨材料,电解液是含有固定比例锂盐的有机碳酸酯溶液。在放电过程中,锂离子从负极材料脱出进入电解液,电解液中等量的锂离子嵌入正极材料;在充电过程中,锂离子从正极材料中脱出进入电解液,电解液中等量的锂离子嵌入负极材料。周而复始,电解液和电极材料中的成分没有损失,结构没有发生改变。显然,这样电解池(逆反应)受到的阻力就小得多了。
我们再从电池内部结构和工艺看,
很容易看出,这样的二次电池结构是“对称的”、“均匀的”、电解质是“自由的”,这就使得原电池和电解池的切换在结构上变得更为容易。
小结:二次电池技术出现的时间是相对较晚的。各大企业也纷纷将研发精力放到二次电池上。即便是这样,我们也不能说一次电池最终会被淘汰,因为一次电池最大的优点就是开启包装便可以使用,尤其是在遇到自然灾害,停电或无电等紧急情况时,可以迅速应用于急需的电子产品内。因此,在我们生活中会一直有用武之地的。
假如我们给该电池充电,即一个电解池。此时,氧化物ZnO仍在KOH胶体中,若将其还原为金属锌,该体系中将会发生较大的极化,强行充电会导致部分材料分解,很难复原到原来状态,均匀的锌粉状态也不再现。这就是小时候淘气,硬要给干电池充电,却发现电池发热,鼓包的原因,而不是我们想要的满电状态。
除了工艺和电池内部结构的区别,从材料角度也很容易理解。早期原电池的开发是以活泼性不同的金属开始的,这么容易被人发现的反应,说明热力学角度无需付出太多代价,也就是更容易发生的自发反应,我们懂得一个道理,自发反应越容易,其逆反应往往需要更为苛刻的条件。
随后以最常见磷酸铁锂锂离子二次电池为例。
锂离子电池以碳材料为负极,以含锂的化合物作正极,没有金属锂存在,只有锂离子,这就是锂离子电池。锂离子电池是指以锂离子嵌入化合物为正极材料电池的总称。锂离子电池的充放电过程,就是锂离子的嵌入和脱嵌过程。在锂离子的嵌入和脱嵌过程中,同时伴随着与锂离子等当量电子的嵌入和脱嵌(习惯上正极用嵌入或脱嵌表示,而负极用插入或脱插表示)。在充放电过程中,锂离子在正、负极之间往返嵌入/脱嵌和插入/脱插,被形象地称为“摇椅电池”。
当对电池进行充电时,电池的正极上有锂离子生成,生成的锂离子经过电解液运动到负极。而作为负极的碳呈层状结构,它有很多微孔,达到负极的锂离子就嵌入到碳层的微孔中,嵌入的锂离子越多,充电容量越高。同样,当对电池进行放电时(即我们使用电池的过程),嵌在负极碳层中的锂离子脱出,又运动回正极。回正极的锂离子越多,放电容量越高。
一般锂电池充电电流设定在0.2C至1C之间,电流越大,充电越快,同时电池发热也越大。而且,过大的电流充电,容量不够满,因为电池内部的电化学反应需要时间。就跟倒啤酒一样,倒太快的话会产生泡沫,反而不满。
名词:
电解液是化学电池、电解电容等使用的介质(有一定的腐蚀性),为他们的正常工作提供离子。并保证工作中发生的化学反应是可逆的。



发表回复